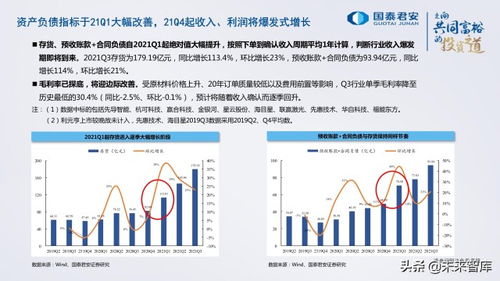
根据Jost Sullivan的数据,仅小核酸药物的全球市场规模就从2016年的0.1亿美元增长到2021年的32.5亿美元,年复合增长率为217.8%。随着未来临床阶段核酸药物的不断上市,将进一步带动市场的快速发展,千亿级核酸药物市场即将开启。但对于国内核酸药物研发企业来说,核酸药物给药技术还有很多问题需要解决,比如非肝脾靶向给药。核酸的输送既是机遇也是挑战。一旦掌握了投放技术的关键,抓住机会就能“一飞冲天九万里”。

1960年,首次成功提取mRNA。2005年,科学家发现经过修饰的mRNA可以逃脱免疫传感器的信号识别,RNA疗法由此诞生。从2010年开始,mRNA技术的研究开始向药物和疫苗方向推进。随着技术的成熟和资本的推动,核酸药物有望成为继小分子药物和抗体药物之后的第三大类药物。但与此同时,传统核酸药物仍存在“制药难”、“无法制药”、“疗效不足”等问题。
核酸药物的研发经历了漫长的过程,其不稳定性、免疫原性、细胞摄取效率低、内吞逃逸困难等缺陷一度制约了核酸药物的发展。特别是对于核酸药物的传递,传递系统是核酸药物能够靶向发挥稳定疗效的保证,也成为影响其药性的最大障碍。有受访者表示,“递送技术是核酸药物尤其是mRNA药物研发的半壁江山。核酸分子是一部分,运载技术是另一部分,缺一不可。”因此,掌握了配送技术的企业成为行业的“香饽饽”。
LNP是核酸药物最广泛使用的递送系统之一。BioNTech、Moderna和CureVac的mRNA新冠肺炎疫苗均采用LNP递送技术。据统计,全球40多个临床mRNA疫苗项目中,有30多个采用了LNP技术。2018年,全球首个siRNA药物Patisiran获批,也是首个采用LNP传递系统的核酸药物。此外,GalNAc技术还在几家制药公司的RD管道中占据重要地位,其中最著名的是Alnylam。Givosiran于2019年11月获得FDA批准,由Alnylam开发,通过增强化学过程稳定ESC-GalNAc组合技术实现皮下给药,具有更高的疗效、持久性和广泛的治疗指数。
是科技公司发展的引擎。对于研发核酸药物的企业来说,一旦掌握了投放技术的关键,抓住机遇就能“一飞冲天九万里”。但是,核酸给药技术还有很多问题需要解决,比如非肝脾靶向给药。目前,LNP和GalNAc已被证明具有较高的传递效率和良好的靶向性。但是,LNP和GalNAc都是基于肝脏特定生物学机制的靶向给药系统,靶向其他组织或细胞的给药技术尚未成熟,目前还达不到LNP或GalNAc的水平。因此,大多数国内核酸药物RD企业都在沿着LNP和GalNAc的原有方向探索。在锐博生物董事长兼CEO梁子才看来,新“进入者”沿着现有方向前行,并不是最好的选择。“如果有些企业现阶段想涉足小核酸的研发,尤其是投放方向,现在花大量精力在GalNAc上可能做不好。还不如重点放在肝外送,他们还能‘争取’。”
因此,业界一直在思考,除了LNP和加尔纳克,交付技术还能取得哪些突破?有受访者表示,目前多种针对肝、肾、眼适应症的候选药物正在临床试验中,针对中枢神经系统和其他非肝组织的新药有望在未来几年实现。
正如圣诺药业创始人杨璐所说,“整个核酸干扰药物领域不能只局限于一种细胞类型。我们应该有更广泛的治疗细胞型疾病的方法。除了肝脏相关代谢疾病,其他领域也要有所突破。这就是我们正在做的。”Q1:递送技术对于核酸药物的研发有什么重要性?
王为民:对于核酸药物来说,递送是开发中最关键的技术。没有传递,就没有核酸药物。大部分核酸药物的作用机制在细胞内,核酸分子本身体积特别大,不容易进入细胞,稳定性不高。因此,基于核酸形式的药物只有通过递送才能制成药物。
付希勇:mRNA的单链结构使其不稳定,容易被降解;也很难穿过表面带负电荷的细胞膜。人体内环境对外源核酸有很强的降解能力。因此,递送技术应该在体外稳定mRNA,在体内保护mRNA,帮助mRNA进入细胞,并及时释放细胞内的mRNA。
mRNA递送技术经过40年的发展,如今只有两种疫苗产品上市,这也说明递送技术的研发难度不容小觑。目前,LNP技术是最流行的传送技术。Q2。肝外靶向给药困难的主要原因是什么?目前交付的前沿发展是什么?

杨璐:事实上,肝脏的运送是“上帝”为我们安排的。肝脏是吸收各种物质的最佳器官。现在,随着研究的深入,发现像我们这样的多肽纳米递送技术不仅可以靶向肝实质细胞,还可以靶向胆汁血管内皮细胞,这是非常重要的。
以GalNAc为例,这项技术实际上只对肝脏中的一种细胞类型极为有利,而这个靶点就是肝实质细胞。所有与肝实质细胞相关的疾病都可以通过这项技术进行治疗。然而,核酸干扰药物的整个领域不能仅限于一种细胞类型。我们需要更广泛的细胞型疾病的治疗方法。除了与肝脏相关的代谢疾病,我们还需要在其他领域取得突破。这就是我们正在做的。
李进:目前核酸药物主流的LNP技术和GalNAc技术都是基于肝脏特定的生物学机制的靶向给药系统。靶向其他组织或细胞的递送技术尚未成熟,目前还没有达到LNP技术或GalNAc技术的水平。核酸起治疗作用,高效安全的输送是关键。未来有望在以下几个方面实现突破:一是靶向肝外器官,如中枢神经系统给药、肺部给药和靶向免疫细胞给药;二是实现更高效低毒的传递,如增强内体逃逸、靶向配体偶联、外体传递等。第三,通过注射以外的其他途径给药。宋:核酸药物是带负电荷的生物活性大分子,靶向能力和穿透细胞膜的能力极差。然而,因为肝脏具有快速摄取游离寡核苷酸和较大纳米颗粒的能力,并且含有高浓度的受体,所以寡核苷酸具有肝脏的天然靶向能力。然而,肝外给药仍然是核酸药物需要面对的主要挑战之一。未来要解决其他组织的靶向输送问题,将从以下几个方面寻求突破:一是化学修饰的输送策略;二是生物耦合的传递策略;三是脂质体偶联给药策略;第四种是叶酸受体介导的靶向给药;最后一个是外泌体传递技术。具有稳定性好、安全性高、免疫原性低、靶向特异性好的特点。目前,一些相关药物已经进入临床研究阶段。
王为民:对于小核酸药物,肝脏给药的技术已经比较成熟,并且已经得到人体验证,这也是小核酸领域能够有大发展的原因。但肝外给药平台还处于研发初期,至今没有真正能临床验证的小核酸药物。尽管如此,现在可以看到一些好的趋势,不同的公司在尝试不同的方向,并取得了一些大的突破和进展。我认为在不久的将来,肝外给药的技术平台会有突破性的发展。梁子才:核酸药物首先突破肝脏,有生物学原因,也有偶然原因。生物学是因为肝脏是机体的解毒器官,很多脂质体、纳米颗粒或其他聚合物容易在肝脏中堆积。偶然的原因是发现了GalNAc作为脱氧唾液酸受体在肝脏特异性小核酸递送的应用。
所以在生物学上,任何肝外靶向给药都需要考虑避免肝脏富集。目前包括我们在内的很多公司在中枢神经、肺部、肿瘤等方面都有一定进展,但还没有肝小核酸传递成熟。但我的预测是,未来2~3年我在一个组织里,能够实现像GalNac那样的突破,几乎每3~5年就会有一次这样的突破。这样,核酸药物的发展也会形成一个循序渐进的发展模式。
Q3:贵公司目前采用哪种交付技术?有什么优势?
杨璐:现在已经证实,中药的投放平台是LNP和GalNAc。我们的PNP也是整个核酸干扰药物领域的重要技术平台。与LNP相比,PNP实际上有它的优势。一个是整个生产过程相对简单,在安全性和有效性方面有更好的应用场景。
事实上,作为发现之源,PNP技术并不是一个固定线程的系统,它具有持续优化的能力。在药物导入方面有更广阔的应用前景。比如我们的STP705的结构是专门用于局部用药的,STP707的另一个结构是专门用于全身用药的,所以它的应用场景应该更广泛。
梁子才:目前我们的肝脏输送手段主要是自主研发的RiboGalSTARTM小核酸输送平台。我们对这个技术平台有着全球性的兴趣。在肝外递送中,我们的主要焦点是小核酸的配体介导的递送。它是传递技术,但它实际上是一个集成小核酸药物开发中各种技术的平台。因为我们多年积累了大量的知识和技术,我们可以完成这个整合,这是我们的优势。
宋庚申:公司LNP传递系统重要专利“一种阳离子脂质化合物,包括其组成和用途”,2022年4月在中国获得授权,2022年1月提交PCT申请。主要保护一系列具有全新化学结构的可电离阳离子脂质以及以它们为主体制备的LNP组合物。公司的LNP由四种成分组成:阳离子脂质、胆固醇、辅助脂质和PEG修饰脂质,其中核心成分是公司发明专利中全新化学结构的可电离阳离子脂质。本公司的LNP组合物具有可生物降解、安全性好、输送效率高、核酸药物稳定性好等优点。,大大提高了核酸药物的给药水平。成分比例规避国外核心专利。
王为民:我们的主要交付平台基于耦合技术。在多年的研发过程中,我们发现可以完全定性为单一化学体,这在药物研发中是一个特别突出的优势。由于表征的形式,可以更有利于在药代动力学、降解产物、药理研究、临床研究、生产等环节进行跟踪和优化。
傅希勇:在递送技术方面,E-Wei Medicine已经获得Acuitas公司的mRNA递送专利许可和技术转让,将进一步合作研发mRNA疫苗和其他疾病药物的脂质体递送系统。E-medicine希望使用经过商业验证的交付技术,以确保早期产品能够高效、高质量地开发出来。
Q4:中国的交付技术现状如何?

梁子才:其实国内对投放技术的研究还是很多的,无论是从学术角度还是从产业角度。在我看来,我们是唯一在GalNAc平台上已经成熟的公司。还有其他几个处于不同的探索和推广阶段。过去,国内的许多努力都集中在LNP和纳米颗粒上,其中一些可能会转化为mRNA递送方法。如果一个企业想在现阶段涉足小核酸的研发,尤其是投放技术方向,可能现在还做不好GalNAc。还不如重点放在肝外送,还是有可能“争取”的。避免低效的内卷化,努力成为全球领导者,应该是大家努力的方向。
张培卓:在未来的发展中,应该说小核酸药物领域可能会走这条路,就是针对不同的细胞,寻找这种可以特异性作用于某一类细胞的靶点,然后通过内吞作用带入。